:::::::::::::::::::::::::::::::::::::::::::::: LE CYCLE DE L'AZOTE
::::::::::::::::::::::::::::::::::::::::::Les pierres vivantes ont été préparées puis mises dans le bac, sans souci esthétique pour l’instant mais en veillant à ce qu’elles soient brassées du mieux possible et de façon à pouvoir siphonner la majorité des sédiments qu’elles vont libérer.
Il sera préférable, pour ceux qui veulent mettre du sable comme substrat de fond dans leur aquarium, d’attendre la fin du premier mois avant son installation, en veillant bien à éliminer tous les sédiments au préalable et à profiter de ce moment pour créer le décor désiré.
De nombreuses réactions vont se produire et favoriser l’établissement des acteurs du cycle de l’azote pendant les premières semaines.
Ces pierres vivantes ont été sorties de leur eau native, ce qui a entraîné la mort et la décomposition de nombreux organismes sous forme de déchets organiques. C’est une source d’énergie qui va déclencher la prolifération d’une première vague de bactéries aérobies, transformant l’azote organique en azote ammoniacal.
C’est l’ammonisation :
Cette première étape va fournir à son tour la matière nécessaire au développement d’autres bactéries, qui vont oxyder les ions ammonium en nitrites.
C’est la nitrosation :
Les nitrites à leurs tour, permettent alors l’établissement de bactéries qui les oxydent en nitrates.
C’est la nitratation :
Ces deux actions, nitrosation et nitratation, constituent la nitrification.
Puis, encore d’autres bactéries qui vont spontanément réduire par étapes successives, ces nitrates en azote gazeux, bouclant ainsi le cycle de l’azote.
C’est la dénitrification :
Qui se réalise dans les milieux pauvres en oxygène, par exemple à l’intérieur des pierres vivantes et dans les lits de sable.
En fonction de la quantité d’énergie fournie par chaque étape du cycle de l’azote, des populations bactériennes différentes se développent pour former les premiers colons de taille microscopique.
Chacune de ces phases pourra être suivie à l’aide de tests aquariophiles, particulièrement les tests des concentrations en nitrites et nitrates.
Ils permettent de suivre les pics successifs, consignés dans un « carnet de bord » et de déterminer le moment propice à l’introduction des premiers habitants de l’aquarium (poissons et invertébrés herbivores et détritivores).
Le test de la concentration en nitrates devrait annoncer une valeur indétectable avant le début du peuplement.
Il faut compter environ un mois pour arriver à ce stade.
Pour l’épuration, la méthode berlinoise repose sur deux piliers que sont les supports biologiques, pierres vivantes, sable vivants et l’écumeur qui retire de l’eau une grande partie des composés organiques dissous avant leurs transformations en nutriments (nitrates, phosphates).
L’écumeur sera mis en route dès le premier jour.
Utiliser du charbon actif, de la meilleure qualité (donc dépourvu de phosphate), sera bénéfique pour éliminer les toxines et les colorants organiques jaunâtres.
L’utilisation passive du charbon immergé consiste à en déposer une grande quantité, jusqu’à 500 g pour 100 litres, dans un sac au fond de la cuve technique et à renouveler cette dose tous les deux à trois mois.
Les réacteurs à lit fluidifié permettent désormais d’utiliser plus efficacement des quantités moindres (50 à 100 g pour 100 litres) qu’il faut en revanche renouveler plus souvent.
La compensation d’eau évaporée pourra se faire avec de l’eau de chaux, elle reconstitue le pouvoir tampon mis à mal par la production d’acide liée à l’épuration naturelle des déchets.
Elle neutralise le dioxyde de carbone disponible pour le développement des algues indésirables et elle précipite les phosphates dissous.
Le cycle de l'azote est un cycle biogéochimique qui décrit la succession des modifications subies par les différentes formes de l'azote (diazote, nitrate, nitrite, ammoniac, azote organique).
Sous forme de nitrate ou d'ammoniaque, l'azote est très soluble et dans l'eau et mobile dans les écosystèmes. Le ruissellement, l'érosion et les pluies tendent à ramener les nitrates non captés par la biomasse terrestre vers les lacs et surtout vers les nappes phréatiques et les océans. Dans la mer, comme sur terre, l'azote dissous dans l'eau est capté (via la photosynthèse) par les plantes et certaines bactéries, puis concentré dans le réseau trophique sous forme de protéines animales notamment.
Tout poisson et tout animal marin concentre dans sa biomasse (matière organique) une partie de l'azote accumulé par les végétaux ou animaux qu’il a consommés, lesquels l’ont prélevé dans le stock océanique, alimenté par l’atmosphère, et de plus en plus excessivement par les apports terrigènes (engrais, et eaux usées essentiellement).
Or, depuis le développement de la pêche industrielle et intensive, cette quantité n’est plus négligeable. En effet, chaque poisson pêché en mer correspond donc à un retrait d’azote du compartiment océanique. Cette quantité a été évaluée pour 58 écosystèmes marins répartis sur le globe par une étude1 récente sur le cycle de l'azote dans les régions côtières. En 1960 la pêche en mer ramenait vers la terre 60 % des composés azotés estimés être apportés par les fertilisants lessivés par les pluies. Or, de 1960 à 2004, ces apports azotés ont été multipliées par 7,5, alors qu’en raison d’une raréfaction des espèces commercialisables suite à la surexploitation des océans, les prises de pêche n’ont augmenté que de 2,5. Seulement environ 20 % de l’azote perdu en mer par l’agriculture sont donc en 2008 « récupérés » par les activités de pêche, laquelle devrait être pour ces raisons mieux prise en compte dans les calculs des bilans d’azote et risques d’eutrophisation.
Une interprétation facile et rapide de ces résultats serait de croire qu’en augmentant encore la pêche on diminuerait l’eutrophisation marine. Cette piste serait illusoire, rappelle Greenpeace l'auteur de l'étude elle-même, notamment parce que poursuivre la surpêche conduira rapidement à la disparition pure et simple de la plupart des espèces commerciales, et donc à une eutrophisation pire encore. La solution préconisée par les ONG environnementales et de nombreux organismes scientifiques, et notamment par un rapport récent2 du Conseil de la recherche portant sur la « qualité de l'eau du fleuve Mississippi au regard de la Loi sur l'eau : progrès, défis et opportunités ». Ce rapport recommande que l'EPA et l'USDA coopérèrent mieux pour réduire les impacts de l'agriculture sur la qualité de l'eau du Mississippi et du nord du golfe du Mexique (zone morte de 22 000 km2 environ en 2007-2008 ; la plus vaste du monde). L'excès d'azote cause la prolifération de phytoplancton qui se décompose en consommant l'oxygène dissous dans l'eau aux dépens des organismes vivants qui disparaissent alors3. La seule solution durable serait de limiter en amont les pertes d’engrais azotés d'origine agricole et de reconstituer un stock de poisson suffisant pour alimenter une pêche durable. Les indicateurs disponibles laissent penser que ces deux options peinent à se mettre en place.
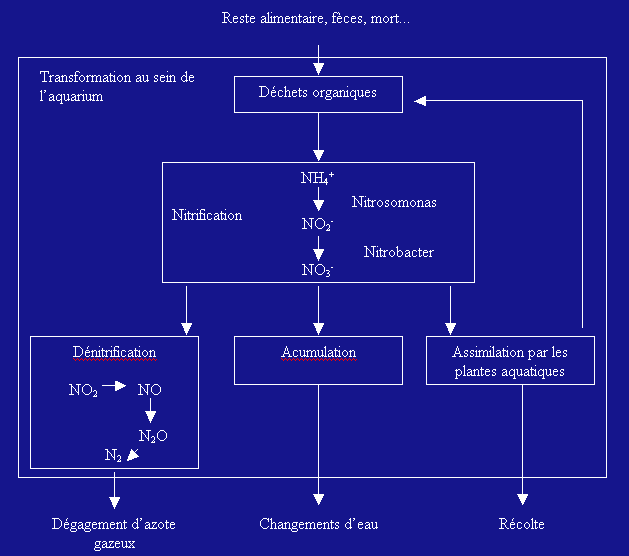
Dans un aquarium, ce sont les déjections des poissons et la nourriture non consommée qui sont à l'origine de la formation d'ammoniac. Ce produit extrêmement toxique pour les animaux aquatiques est transformé en nitrates beaucoup moins toxiques et bénéfiques pour les plantes par des bactéries présentes naturellement ou artificiellement (plantées) dans l'aquarium.
Les bactéries nitrosomonas transforment l'ammoniac en nitrites, eux-mêmes très toxiques pour les animaux aquatiques. Et les bactéries nitrobacter transforment les nitrites en nitrates. Nitrates qui sont alors absorbés par les plantes présentes dans l'aquarium.
Lors du premier remplissage de l'aquarium, ces bactéries sont absentes de l'eau. Les populations de bactéries apparaissent progressivement à partir du moment où l'aquarium est rempli. Le lancement du cycle nécessite, selon le contexte, entre trois et 8 semaines durant lesquelles l'eau de l'aquarium reste toxique. L'accumulation d'ammoniac provoque la prolifération de la première population de bactéries. Ces bactéries transforment l'ammoniac en nitrites. Au bout de quelques jours l'accumulation de nitrites due à la première population de bactéries provoque la prolifération de la deuxième population de bactéries, qui fait retomber la concentration de nitrites. La concentration de nitrites redescend jusqu'à être totalement indétectable. À partir de ce moment, l'aquarium est sain pour les poissons.
La plupart des aquariums ont un excédent de poissons, et pas assez de plantes par rapport à la quantité de nitrates produites. Les nitrates finissent par s'accumuler dans l'eau, et il est alors nécessaire de les diluer régulièrement au bout de une à deux semaines en remplaçant une part de l'eau de l'aquarium par de l'eau « neuve ». La fréquence des remplacements dépendra de la sensibilité des animaux. De nombreux poissons supportent des concentrations jusqu'à 50 mg/L. Par contre, les coraux « durs » ne supportent pas des concentrations supérieures à 2 mg/L.
Les bactéries dégradant l'ammoniac et les nitrites sont présentes dans l'eau, le sol de l'aquarium et le filtre. Le brassage provoqué par le filtre et la pompe amène l'eau riche en oxygène de la surface vers le fond, et assure la survie des bactéries - qui ont besoin d'oxygène pour vivre. Il sert également à mettre en contact les bactéries présentes dans le filtre avec l'eau de l'aquarium.
À partir du moment où le cycle de l'azote est en route, on dit que l'aquarium est cyclé : l'ammoniac et les nitrites qui se forment dans l'eau sont immédiatement transformés, et les concentrations restent à des niveaux indétectables.
les sources
1: zebrasomag
2 et 3 wikipedia



